反義寡核苷酸(ASOs)領域是一個新興的藥物開發領域,自1978年ASOs概念出現,經過20多年的發展,ASOs才被開發成可用于商業用途的藥物。ASOs可以與靶基因配對,通過特異性阻斷靶基因的轉錄或翻譯過程來實現基因調控。ASOs藥物具有高特異性、高效率、低毒等優點,廣泛應用于基因功能研究、藥物靶點驗證、和腫瘤治療等領域。
已上市的ASOs藥物
|
Drug |
Approval year |
Target Indication |
Target gene |
Mode of action |
Chemistry |
|---|---|---|---|---|---|
|
Formivirsen |
1998 |
CMV retinitis |
CMV |
RNase H1 |
PS-ODN |
|
Mipomersen |
2013 |
HoFH |
ApoB-100 |
RNase H1 |
PS-MOE gapmer |
|
Nusinersen |
2016 |
SMA |
SMN2 intron 7 |
EXON inclusion |
PS-MOE |
|
Eteplirsen |
2016 |
DMD |
Dystrophin exon 51 |
EXON skipping |
PMO |
|
Inotersen |
2018 |
hATTR |
TTR |
RNase H1 |
PS-MOE gapmer |
|
Golodirsen |
2019 |
DMD |
Dystrophin exon 53 |
EXON skipping |
PMO |
|
Volanesorsen |
2019 |
FCS |
ApoC-III |
RNase H1 |
PS-MOE gapmer |
|
Viltolarsen |
2020 |
DMD |
Dystrophin exon 53 |
EXON skipping |
PMO |
|
Casimersen |
2021 |
DMD |
Dystrophin exon 45 |
EXON skipping |
PMO |
ASOs藥物主要作用機制
ASO藥物根據其作用機制可分為兩類:
RNase H介導的降解:在這種機制中,RNase H1酶識別并切割RNA-DNA樣的異雙鏈結構。為了激活RNase H,ASOs必須包含5到10個連續的脫氧核苷酸,PS連接也能激活RNase H。中心的PS-ODN間隙(8-10個核苷酸)兩側被2′-修飾的核苷酸(如MOE、LNA或cEt)所夾持,這些修飾增加了穩定性和親和力,形成gapmer結構。PS連接和2′修飾會降低RNase H活性,導致這些反義寡核苷酸變為僅占位寡核苷酸,從而調節剪接。
可變剪接:發生在僅占位的寡核苷酸(如nusinersen和PMO類藥物,如eteplirsen、golodirsen、viltolarsen和casimersen)中,這些寡核苷酸與前體mRNA結合并阻止剪接體,誘導外顯子包含或跳過。這一機制用于治療脊髓性肌萎縮癥(SMA)和杜氏肌營養不良癥(DMD)等疾病。
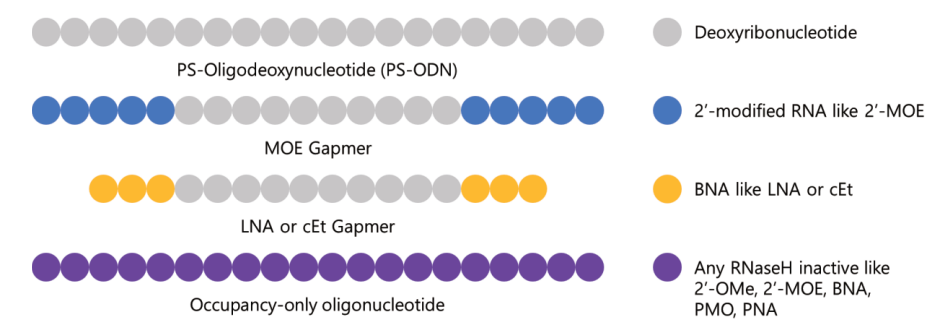
ASOs作用機制圖
ASOs藥物在研發過程中為了確保ASOs藥物的療效和穩定性,可以對其進行ASOs設計、化學修飾等方法,最大限度地提高ASOs藥物的療效,確保其在臨床應用中的安全性和長期有效性。
ASOs設計
ASOs的設計是決定其療效和特異性的核心。設計時主要考慮以下因素:
序列特異性:確保ASOs僅與目標RNA結合,避免與其他基因的非特異性結合。
穩定性與親和力:優化ASOs的化學結構以提高其在體內的穩定性,避免快速降解,同時增強與靶RNA的結合親和力。
抗脫靶效應:確保ASOs對非靶RNA的干擾最小化,減少副作用。
ASOs化學修飾
ASOs主要有堿基修飾、糖修飾和linker修飾。不同修飾各自有助于優化ASOs的治療潛力,可提高ASOs的穩定性、療效和安全性。
Linker修飾:集中于穩定ASOs的骨架,防止外切酶的降解,改善分子的藥代動力學性質。
堿基修飾:影響ASOs與靶RNA的特異性結合,增強親和力和選擇性。
糖修飾:主要通過保護糖骨架不被降解來提高ASOs的穩定性,從而延長其半衰期。
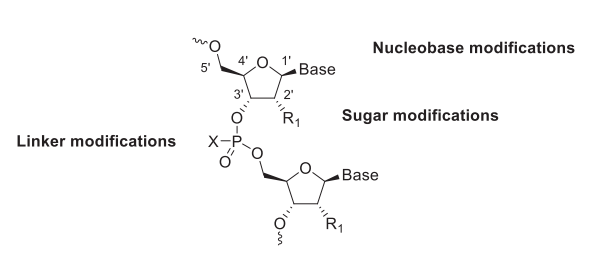
ASOs化學修飾
ASOs經過化學修飾之后,大大地提高穩定性、靶向性,減少降解產物,最大限度降低不良反應的可能性,提高 ASOs的整體安全性。
ASOs藥物的臨床應用
1. 脊髓性肌萎縮癥(SMA)
SMA是由于SMN1基因功能缺失引起的,SMN2基因雖然產生一定量的全長SMN蛋白,但由于外顯子7跳過,常常產生短小且不穩定的蛋白。Nusinersen是一種2′-MOE修飾的PS ASO,通過促進SMN2前體mRNA的外顯子7包含,從而恢復全長SMN蛋白的產生。
2. 杜氏肌營養不良癥(DMD)
DMD是由于基因的突變導致其閱讀框破壞,產生提前的終止密碼子,導致基因表達中斷。Eteplirsen通過與DMD前體mRNA的外顯子51結合并使其跳過,從而恢復功能性,但較短的肌營養不良蛋白。同樣,golodirsen和viltolarsen通過與外顯子53結合,casimersen通過與外顯子45結合,促使這些外顯子跳過,恢復肌營養不良蛋白的表達。
3. 肌萎縮側索硬化癥(ALS)
ALS也稱漸凍癥,ALS患者常伴有進行性肌肉無力及消瘦癥狀,具有局灶性發作并擴散至身體不同區域,常因呼吸肌衰竭致死 。2023年4月,美國FDA加速批準治療SOD1相關ALS的ASOs藥物Tofersen(商品名:Qalsody)上市。Tofersen通過誘導RNase H介導SOD1 mRNA降解,以減少ALS 患者SOD1蛋白的合成,使患者腦脊液SOD1濃度以及血漿中受損神經元釋放的神經絲輕鏈濃度的顯著降低,患者呼吸功能和肌肉力量的下降速度得到改善 。
4. 遺傳性轉甲狀腺素蛋白介導的淀粉樣變多發性神經病變(ATTRv-PN)
轉甲狀腺素蛋白(transthyretin,TTR)是一種血漿載體蛋白,可運載甲狀腺素和維生素A至全身各個組織和細胞。ATTRv-PN是一種TTR突變引起的以周圍神經損害為主的多系統疾病,其特征是TT不穩定性水解、錯誤折疊并引起淀粉樣蛋白原纖維在細胞外沉積導致細胞被破壞,進而引起周圍神經系統為主的損害,干擾組織的正常功能。Eplontersen通過3 個N-乙酰半乳糖胺(Nacetylgalactosamine,GalNAc)配體靶向肝臟組織,與野生型及突變型TTR mRNA結合并誘導RNase H介導其降解以減少循環TTR蛋白,從而降低患者淀粉樣蛋白的沉積水平。
泓迅生物ASOs合成服務
泓迅生物建立了符合ISO9001和ISO13485質量管理要求的生產車間,擁有標準的生產流程,精湛的合成及純化工藝。合成的ASOs均嚴格執行QC檢測標準,通過HPLC純度檢測,以確保高質量的ASOs產品輸出。
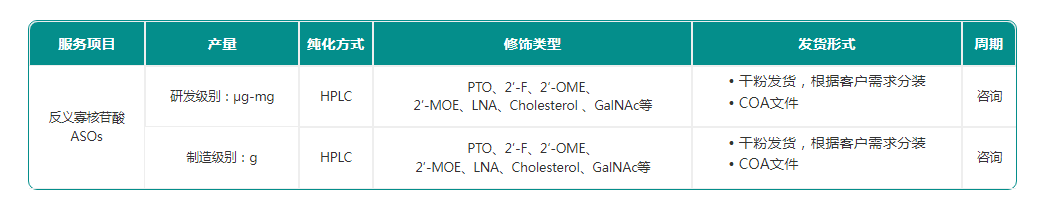
服務優勢
1. 豐富的修飾類型
2. μg-g合成規格
3. HPLC和LC-Mass分析
參考文獻:
1.Kim Yeonjoon. Drug Discovery Perspectives of Antisense Oligonucleotides[J]. Biomolecules & Therapeutics,2023,31(3):241-252. doi:10.4062/biomolther.2023.001
2.Echevarría Lucía, Aupy Philippine, Goyenvalle Aurélie. Exon-skipping advances for Duchenne muscular dystrophy[J]. Human Molecular Genetics,2018,27(R2):R163-R172. doi:10.1093/hmg/ddy171
3.胡祎瑄, 周子凱. 反義寡核苷酸藥物在神經系統疾病治療中的研究與應用[J]. 中國醫藥導刊,2024,(04):30-37.
 Syno?C 引物合成
Syno?C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno?GS 基因合成
Syno?GS 基因合成 載體構建
載體構建 高通量及DNA文庫構建
高通量及DNA文庫構建 CRISPR基因編輯平臺
CRISPR基因編輯平臺 病毒包裝
病毒包裝 基因測序及分析
基因測序及分析 重組蛋白表達平臺
重組蛋白表達平臺 抗體工程平臺
抗體工程平臺 多肽服務
多肽服務 生物信息學分析與設計
生物信息學分析與設計 CRISPR文庫
CRISPR文庫 ProXpress蛋白快速檢測
ProXpress蛋白快速檢測 CRISPR 質粒
CRISPR 質粒





















